
Annex 1: Camere bianche e ambienti a contaminazione controllata
Annex 1: Camere bianche e ambienti a contaminazione controllata
Annex 1: Camere bianche e ambienti a contaminazione controllata
Articolo a cura del team Commissioning & Qualification S4BT.
Nella manifattura di prodotti sterili, rivestono particolare importanza le camere bianche e il grado di pulizia in esse raggiunto. In questo articolo approfondiamo il tema della qualifica e riqualifica in ambito GMP.
Cosa occorre per ottenere un grado di pulizia appropriato?
Sicuramente è necessario partire da una buona progettazione e realizzazione.
1. Superfici
Nelle camere bianche tutte le superfici esposte come i piani di lavoro o le pareti dei locali dovrebbero essere lisce e di facile accesso in modo da ridurre al minimo l’accumulo di particelle contaminanti e permettere una quanto più comoda pulizia.
2. Spazi e ingombri
La progettazione ideale richiede che non ci siano rientranze, sporgenze, scaffali o armadi e che la presenza di altri tipi di qualsivoglia attrezzatura sia ridotta al minimo indispensabile.
3. Porte e Soffitti
Tale principio si applica anche alla progettazione delle porte, che dovrebbero essere realizzate in modo da evitare recessi di difficile pulizia.
Allo stesso modo i soffitti dovrebbero essere progettati e sigillati per prevenire la contaminazione dallo spazio sovrastante.
A tutte queste considerazioni, si aggiunge ancora la corretta progettazione del sistema HVAC e l’utilizzo dei filtri HEPA, attraverso i quali l’aria trattata viene opportunamente immessa nel locale.
Che cos'è Annex 1?
Annex 1 è un allegato delle EudraLex – Volume 4 – Good Manufacturing Practice (GMP) guidelines, dedicato alla fabbricazione di prodotti sterili. Tuttavia alcuni principi e linee guida, come la strategia di controllo della contaminazione, la progettazione dei locali,
la classificazione delle camere bianche, la qualificazione, la convalida, il monitoraggio e la vestizione del personale, possono essere utilizzati per supportare la fabbricazione di altri prodotti non destinati alla sterilità, come determinati liquidi, creme, unguenti e intermedi biologici a bassa carica microbica, ma per i quali il controllo e la riduzione della
contaminazione microbica, particellare e da endotossine/pirogeni è considerato importante. Nel 2022 l’Annex 1 è stato revisionato.
Annex 1: 4 gradi di pulizia
L’Annex 1 fa riferimento ad una classificazione delle camere bianche e degli ambienti a contaminazione controllata che prevede quattro gradi di pulizia:
- GRADO A: sono le zone critiche per le operazioni ad altro rischio, come linee di lavorazioni asettiche, zone di riempimento, piani di lavoro con ampolle e flaconi aperti;
- GRADO B: dedicate alla preparazione e al riempimento asettico. Sono solo e soltanto le zone che circondano quelle di grado A;
- GRADO C e D: zone utilizzate per l’esecuzione di fasi meno critiche nella fabbricazione di prodotti sterili riempiti asetticamente.
Nei sistemi a flusso d’aria unidirezionale, tipici delle zone di grado A, un adeguato movimento d’aria fornisce la protezione del prodotto e dei componenti aperti all’altezza del piano di lavoro (ad esempio dove sono condotte le operazioni ad alto rischio e dove il prodotto e i componenti sono esposti).
Qualifica di Camere Bianche e attrezzature per aria pulita
La qualifica viene intesa come il processo globale di valutazione del livello di conformità di una camera bianca classificata o di un’attrezzatura per l’aria pulita con il suo uso previsto.
Come tutti i sistemi e le apparecchiature aventi impatto GxP, anche la qualifica delle cleanrooms dovrà seguire i requisiti e l’approccio alla qualifica descritti nella normativa di riferimento Annex 15 Qualification and Validation.
9 Test necessari per verificare la conformità di una camera bianca
Al fine di verificare la conformità di una cleanroom vengono considerati necessari almeno i seguenti test di verifica:
1. Test di integrità dei filtri installati
Questo test viene effettuato per assicurare che i filtri siano installati correttamente verificando l’assenza di perdite o di difetti e che sul telaio del filtro ci sia perfetta tenuta.
Vengono introdotte particelle di aerosol a monte del filtro tramite un generatore e ne viene misurata la concentrazione.
Viene poi effettuata una scansione a valle del filtro per misurarne la penetrazione tramite due modalità: attraverso l’uso di un fotometro o tramite l’uso di un contaparticelle.
Il limite massimo di penetrazione accettabile è lo 0,01%, come da indicazione della normativa ISO 14644-3.
2. Misurazione del flusso d’aria – portata e velocità (la velocità viene misurata nei sistemi a flusso unidirezionale)
Questo test viene eseguito per misurare il flusso d’aria introdotto in camere bianche a flusso unidirezionale e non unidirezionale.
Nelle applicazioni a flusso unidirezionale, la velocità del flusso d’aria, che dovrebbe ricadere all’interno dei valori guida 0,36 – 0,54 m/s, è misurata in diversi punti della superficie del filtro e del piano di lavoro tramite ad esempio, un anemometro a filo caldo, al fine di dimostrarne l’uniformità.
Nelle zone a flusso non unidirezionale è possibile misurare direttamente la portata di aria utilizzando ad esempio un balometro, dotato di un convogliatore del flusso d’aria; il dato rilevato potrà essere utilizzato per il calcolo del numero di ricambi orari (volumi di aria nell’unità di tempo).
3. Misurazione della pressione differenziale tra i locali
Lo scopo del test della differenza di pressione dell’aria è quello di verificare la capacità del sistema di mantenere il differenziale di pressione specificato tra la camera bianca e l’ambiente circostante o tra camere bianche di grado diverso, in modo da non permettere contaminazione incrociata. Tale verifica viene effettuata con il supporto di un micromanometro differenziale.
4. Direzione e visualizzazione dei flussi d’aria
Il test della visualizzazione del flusso d’aria può essere condotto nello stato di riposo per determinare i modelli di base del flusso d’aria della camera bianca e può essere ripetuto nello stato dinamico simulando le operazioni reali. Questa verifica è necessaria per dimostrare che non c’è ingresso dalle aree di grado inferiore a quelle di grado superiore e che l’aria non transiti da aree meno pulite (pavimento) alle aree di grado superiore (piani di lavoro).
Inoltre la visualizzazione dei flussi d’aria consente di apportare migliorie al design della cleanroom, di individuare disomogeneità della velocità del flusso, di valutare correttamente la posizione dei punti di monitoraggio ambientale e di addestrare gli operatori riguardo alle corrette modalità di svolgimento delle operazioni asettiche.
5. Contaminazione particellare
Parte integrante della qualifica di una camera bianca è proprio la sua classificazione: è un metodo per valutare il livello di pulizia dell’aria rispetto a una specifica di riferimento (vedi tabella 1), misurando la concentrazione di particolato aerodisperso.
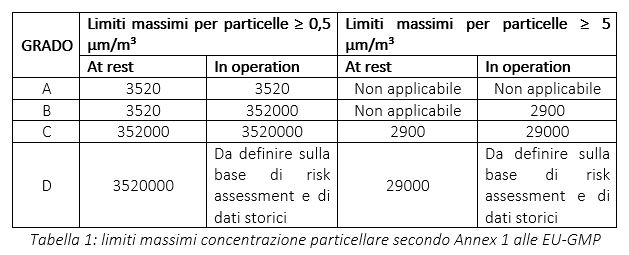
Per gli ambienti di grado A (nello stato occupazionale “at-rest” e “in operation”) e di grado B (nello stato occupazionale “at-rest”) non sono stati ritenuti applicabili i limiti di concentrazione per le particelle da 5 μm; pertanto, possono essere prese in considerazione particelle di dimensione maggiore o uguale a 1 μm, secondo i limiti indicati dalla norma ISO 14644-1.
Per la classificazione delle camere bianche, il numero minimo di punti di campionamento da effettuare e il loro posizionamento sono definiti nella normativa ISO 14644-1.
Nel caso di manifattura sterile e ambienti ad essa collegati (zone di grado A e di grado B), le posizioni dei punti di campionamento devono essere definite considerando anche tutte le zone critiche di lavorazione.
A tal proposito si rende necessaria un’attività di valutazione del rischio documentata sulla base della conoscenza del processo e delle operazioni da eseguire.
6. Contaminazione microbica dell’aria e della superficie
Lo scopo di questo test è la determinazione della concentrazione di microrganismi presenti nell’aria e sulle superfici attraverso il controllo della contaminazione nelle modalità statica, dinamica e attraverso la misura della contaminazione sulle superfici.
7. Misurazione della temperatura e dell’umidità relativa
Lo scopo di questo test è quello di verificare che i livelli di temperatura e di umidità relativa dell’aria siano entro i limiti di controllo sia nello stato occupazionale “at-rest” che in quello “in operation” per l’area da testare.
A tal proposito vengono effettuate mappature termoigrometriche utilizzando dispositivi di misurazione come i datalogger che rilevano e registrano i valori delle grandezze misurate in diversi punti della cleanroom.
8. Test del “recovery”
Lo scopo del test di recovery time è quello di valutare l’intervallo di tempo effettivo affinché la concentrazione di particelle inquinanti ritorni ad un livello di pulizia target dopo essere stata temporaneamente incrementata di un fattore 100 (o 10). Le particelle sporcanti vengono prodotte da un generatore di fumo e ne viene misurata la concentrazione tramite un contaparticelle.
9. Test di verifica del contenimento
Questo test viene eseguito per rilevare eventuali intrusioni di aria non filtrata nella camera bianca o nelle zone pulite dall’esterno attraverso giunti, porte e soffitti pressurizzati. In accordo alla normativa ISO 14644‑2 dovrebbe essere eseguito ogni quattro anni oppure nel caso di un qualsiasi cambiamento apportato che possa coinvolgere i flussi di aria.
Programma di Riqualifica
Per garantire che una camera bianca operi in conformità con quanto richiesto dalle normative, assicurando sicurezza e qualità del prodotto finale durante tutto il suo ciclo di vita, è necessario pianificare un programma di riqualifica periodica, da effettuare secondo procedure definite.
I test minimi richiesti in fase di riqualifica e la cadenza temporale con la quale dovrebbero essere eseguiti secondo l’Annex 1 vengono riportati nella tabella 2:
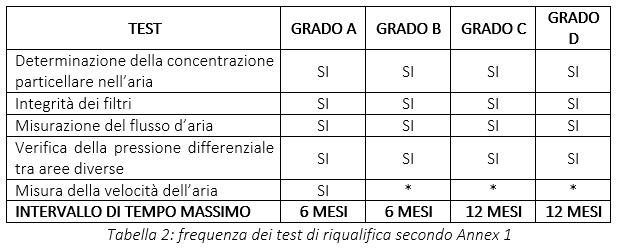
* eseguito secondo una valutazione dei rischi documentata; tuttavia, richiesto per le zone di riempimento e per quelle che circondano le zone di grado A.
Una riqualifica appropriata comprendente almeno le prove di cui sopra dovrebbe essere effettuata anche dopo il completamento di un’azione correttiva attuata per correggere una condizione di non conformità o dopo modifiche apportate.
Casi di modifiche da considerare includono, ad esempio:
- Cambi nell’uso operativo della camera bianca o dei parametri operativi di un HVAC
- Interruzione della movimentazione dell’aria che influisce sul funzionamento dell’impianto.
- Manutenzione speciale che influisce sul funzionamento dell’impianto (come il cambio dei filtri finali).
Altre caratteristiche, come la temperatura e l’umidità relativa, dovrebbero essere controllate entro intervalli che si allineano con i requisiti di prodotto/lavorazione e supportano il mantenimento di standard di pulizia definiti (ad esempio, grado A o B).
La frequenza di esecuzione del test di visualizzazione dei flussi d’aria dovrà essere stabilita all’interno di un processo di valutazione del rischio o qualora siano implementati dei cambiamenti nella configurazione della clean room.
Servizio S4BT Commissioning & Qualification
S4BT fornisce consulenza per la definizione del package documentale relativo al processo basato sul Quality Risk Management (QRM) per la definizione della strategia di Commissioning & Qualification, nonché per l’esecuzione dei test, sfruttando l’esperienza maturata negli anni nelle aziende del settore.
Per maggiori informazioni visita la pagina dedicata: Commissioning & Qualification


